FDA批准Yuviwel那韦培肽(navepegritide)用于治疗儿童软骨发育不全
来源:网络收集 收录时间:2026-03-02热度: ℃
【资讯导读】Yuviwel(那韦培肽,TransCon® CNP)是FDA 加速批准的全球首个、也是目前唯一每周一次给药、可实现持续全身 CNP 暴露的软骨发育不全(ACH)治疗药物,用于促进 2 岁及以上骨骺未闭合患儿
公司: Ascendis Pharma A/S
批准日期: 2026年2月27日
治疗适应症:软骨发育不全
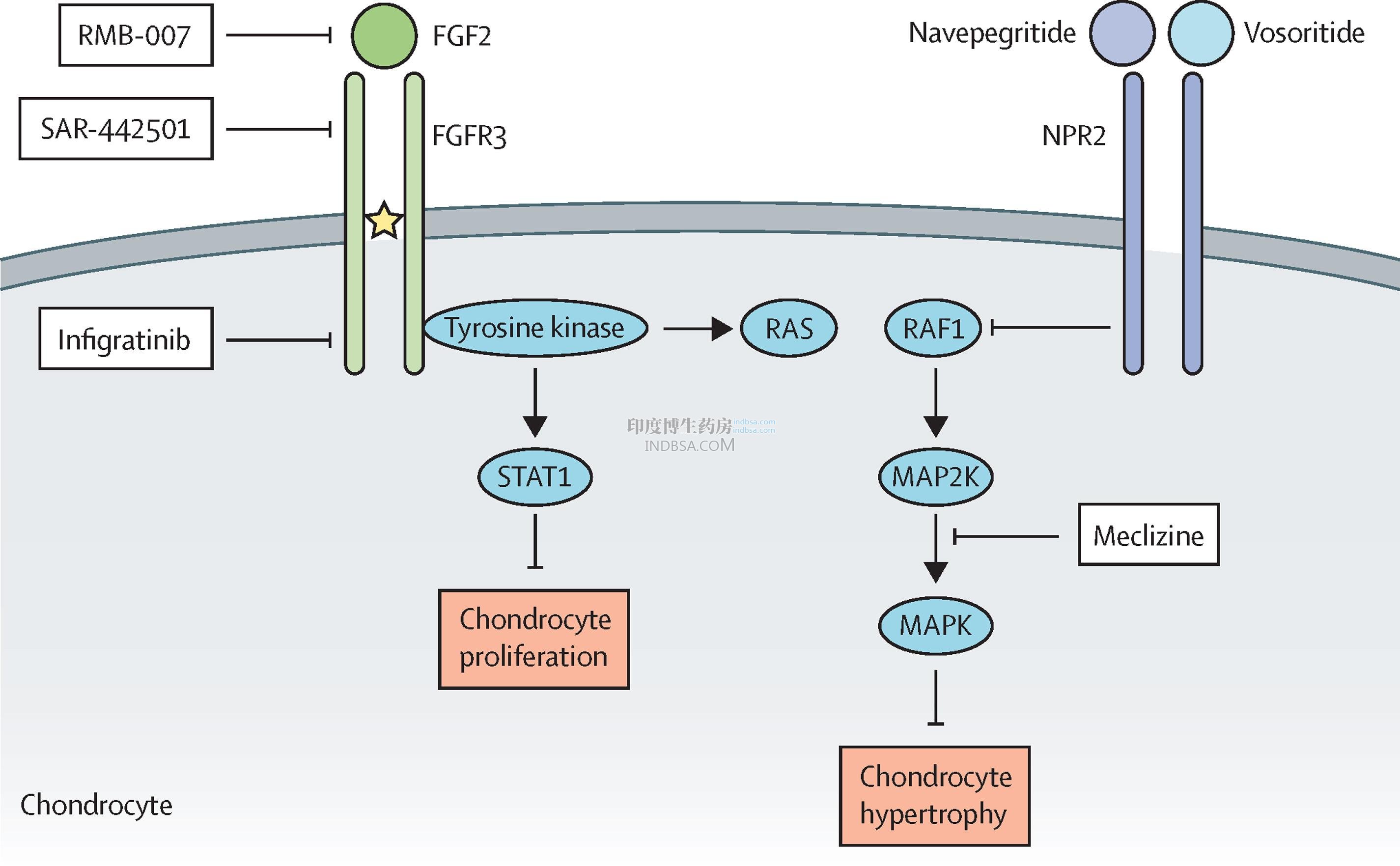
Yuviwel(navepegritide)是一种 C 型利钠肽类似物,用于治疗儿童软骨发育不全。
详情预览:
Yuviwel(那韦培肽,TransCon® CNP)是FDA 加速批准的全球首个、也是目前唯一每周一次给药、可实现持续全身 CNP 暴露的软骨发育不全(ACH)治疗药物,用于促进 2 岁及以上骨骺未闭合患儿的线性生长。
一、获批与上市核心信息
-
获批时间:2026 年 2 月 27 日,FDA 加速批准。
-
适应症:2 岁及以上、骨骺未闭合的软骨发育不全儿童,促进线性生长。
-
审批依据:基于年化生长速度(AGV)改善;持续获批需验证性试验确认临床获益。
-
上市时间:2026 年第二季度初,美国上市。
-
技术平台:TransCon®(持续控释),每周 1 次皮下注射。
-
审评奖励:获罕见儿科疾病优先审评券(PRV)。
二、作用机制(精准靶向病因)
软骨发育不全由FGFR3 功能获得性突变导致,过度激活的 FGFR3 抑制软骨内成骨,引发身材矮小与多系统并发症。
-
Yuviwel 是C 型利钠肽(CNP)前体药物,通过 TransCon 技术实现每周持续全身 CNP 暴露。
-
活性 CNP阻断过度活跃的 FGFR3 信号,解除对软骨生长的抑制,促进线性生长。
三、临床价值与优势(填补空白)
-
全球首创周制剂:唯一每周 1 次、持续全身 CNP 暴露的 ACH 治疗方案,大幅提升依从性。
-
精准靶向机制:直接纠正 FGFR3/CNP 通路失衡,从病因层面改善生长。
-
循证数据扎实:基于3 项随机双盲安慰剂对照试验 + 3 年开放标签扩展数据,关键 ApproaCH 试验发表于《JAMA Pediatrics》。
-
全年龄段覆盖:适用于 2 岁至骨骺闭合前的 ACH 患儿,覆盖关键生长窗口期。
四、安全性与使用要点
核心不良反应
-
最常见:注射部位反应(红、痒、肿、痛、瘀伤、水泡等)。
-
严重风险:低血压(头晕、疲倦、恶心),需及时就医。
-
其他:暂未发现其他严重安全性信号,整体耐受性良好。
重要使用提示
-
告知医生患儿肾脏疾病、妊娠 / 哺乳计划及所有合并用药。
-
副作用报告:FDA 1-800-FDA-1088;Ascendis 1-844-442-7236。
五、疾病背景与临床意义
-
软骨发育不全(ACH):最常见遗传性侏儒症,全球超 25 万人受累,常染色体显性遗传,发病率约 1/15,000–1/25,000。
-
核心危害:不成比例身材矮小、四肢短小、巨头、面中部发育不全;伴脊柱异常、睡眠呼吸障碍、听力障碍、心肺并发症等,严重影响生活质量。
-
治疗突破:此前仅伏索利肽(每日注射)获批,Yuviwel 以周制剂 + 持续暴露显著优化治疗模式,为患儿与家庭提供更便捷、更稳定的治疗选择。
六、商业化与患者支持
-
推广:Ascendis 美国团队负责,通过 **Ascendis Signature Access Program (ASAP)** 提供治疗指导与符合条件患者的经济援助。
-
可及性:2026 年 Q2 初通过美国处方医生全面可及。
七、总结
Yuviwel 是软骨发育不全治疗领域的里程碑式突破,以每周一次、持续全身 CNP 暴露的创新方案,解决了现有治疗依从性差、暴露不稳定的痛点,为 2 岁及以上 ACH 患儿提供了更优的线性生长促进选择,显著改善患儿治疗体验与长期预后。
本站部分文章/图片收集于网络!如涉及版权请联系我们核实删除

