Lorecivivint已向FDA提交审批用于治疗膝骨关节炎
来源:网络收集 收录时间:2026-02-26热度: ℃
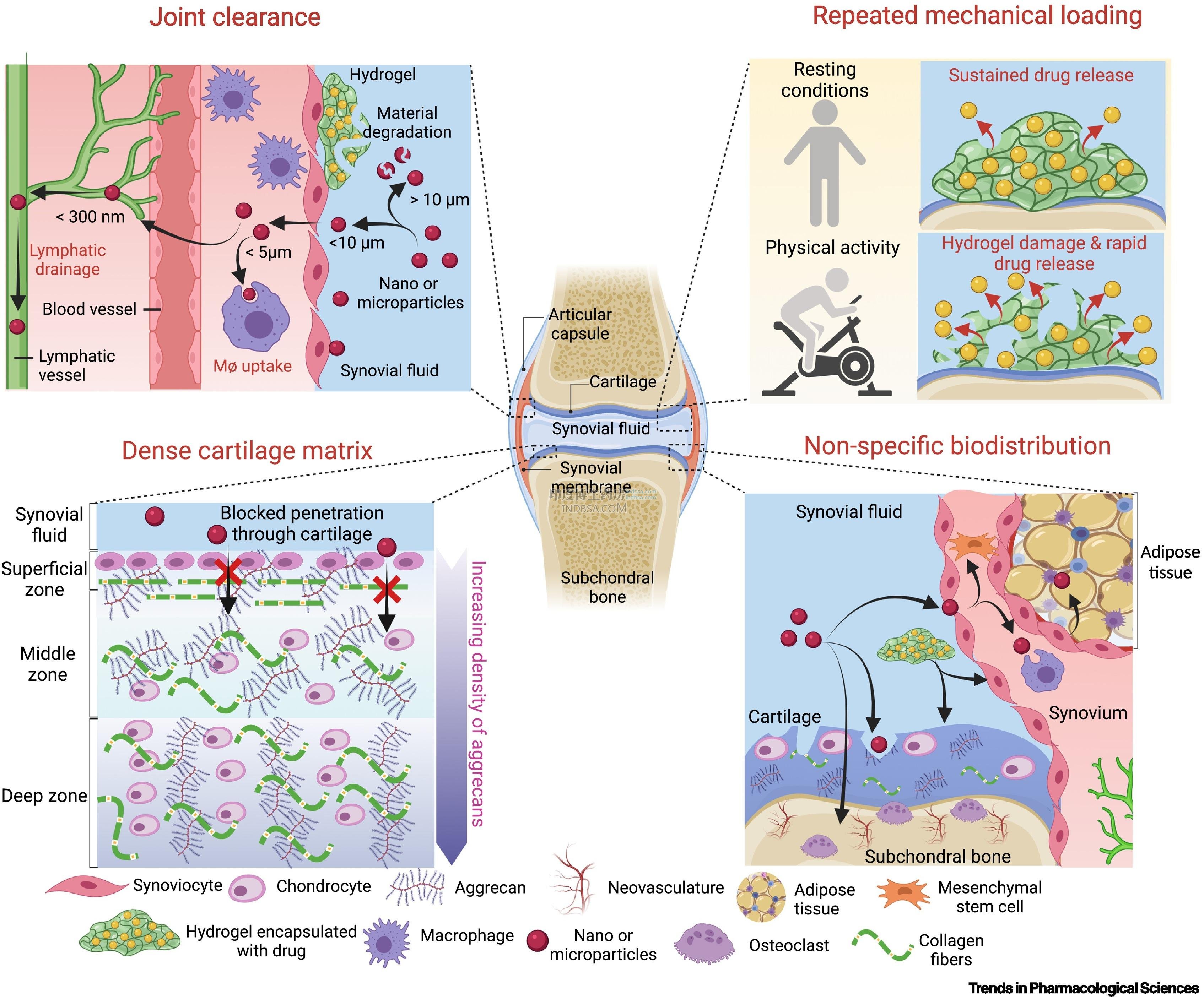
【资讯导读】Biosplice Therapeutics 已于2026 年 1 月 6 日正式向美国 FDA 提交Lorecivivint(LOR,SM04690)用于膝骨关节炎治疗的新药申请(NDA)。这是全球首个进入 NDA 阶段、针对Wnt 通路的疾病改善型骨关节炎
Biosplice Therapeutics 已于
2026 年 1 月 6 日正式向美国 FDA 提交
Lorecivivint(LOR,SM04690)用于膝骨关节炎治疗的
新药申请(NDA)。这是全球首个进入 NDA 阶段、针对
Wnt 通路的
疾病改善型骨关节炎药物(DMOAD),有望填补膝 OA 领域长期缺乏结构改善药物的空白。
一、NDA 核心信息
-
提交时间:2026 年 1 月 6 日
-
申请主体:Biosplice Therapeutics
-
药物:Lorecivivint(LOR),关节内注射小分子混悬液
-
适应症:膝骨关节炎(Knee Osteoarthritis)
-
NDA 依据:11 项临床试验数据,覆盖数千例膝 OA 患者
-
核心价值:首个申报上市的 DMOAD,区别于仅缓解症状的传统疗法,直击软骨退变根源
-
一、药物基本信息
-
通用名:Lorecivivint
-
药物类型:小分子混悬液,关节内注射
-
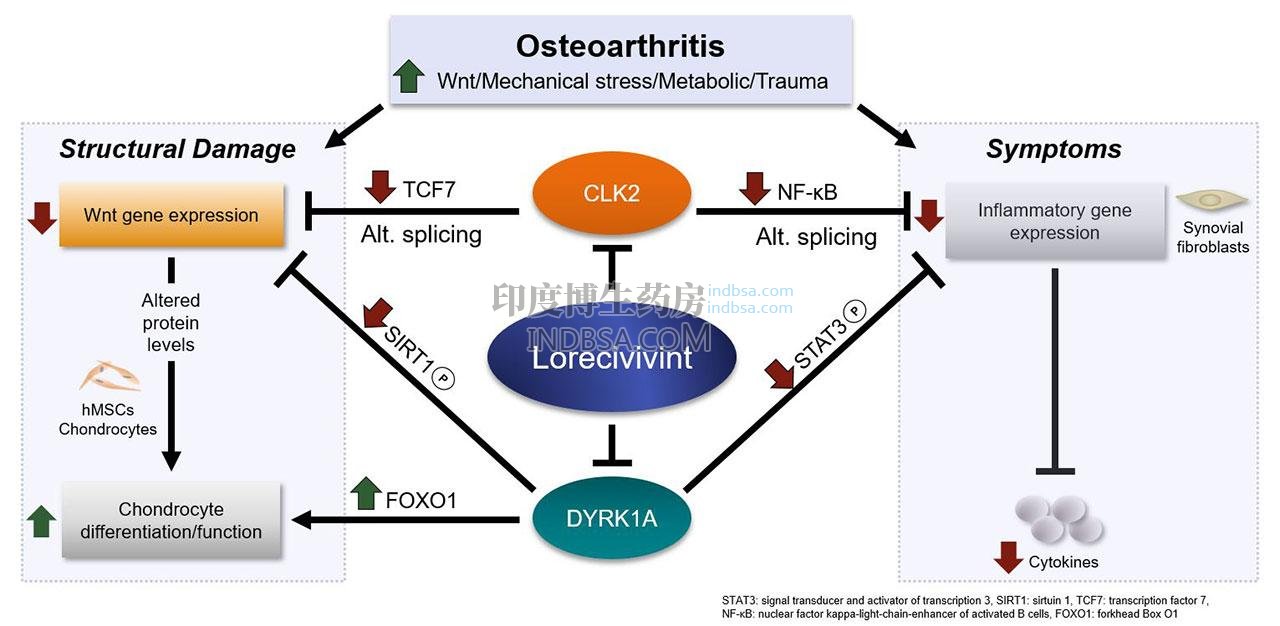
作用靶点:强效、选择性抑制CLK2与DYRK1A双激酶
-
核心机制:调控 Wnt 信号通路,兼具抗炎、软骨保护与再生双重作用
-
抑制DYRK1A:减少炎症因子与分解代谢酶(如基质金属蛋白酶),阻断软骨破坏
-
抑制CLK2:促进软骨细胞分化与成熟,推动软骨修复与再生
-
不影响 β‑连环蛋白,安全性更高
二、临床关键数据(截至 2026‑02‑26)
-
NDA 基础:基于11 项临床试验,覆盖超数千例膝 OA 患者
-
3 期 OA‑07 试验:单次注射后,长期影像学显示内侧关节间隙宽度(JSW)改善,提示延缓关节结构退变
-
2b 期剂量探索:0.07 mg为最优剂量,12 周时显著改善 WOMAC 疼痛与功能评分(P=0.04/0.021);0.23 mg 在 24 周持续获益PubMed
-
长期疗效:单次注射后疗效持续 12 个月,疼痛与功能评分显著优于安慰剂
-
安全性:不良反应发生率与安慰剂相当,无治疗相关严重不良事件,耐受性良好
三、开发与审批进展
-
最高研发阶段:NDA 已提交(美国 FDA),为膝骨关节炎领域潜在首个新机制 DMOAD
-
适应症拓展:同步探索髋、肩关节炎及退行性椎间盘疾病
-
国内进展:与海思科等合作,推进中国临床开发
四、临床价值与意义
-
区别于传统治疗:不同于 NSAIDs、激素仅缓解症状,Lorecivivint直击软骨退变根源,有望延缓 / 逆转疾病进程
-
给药优势:关节腔局部注射,全身暴露低、副作用小
-
未被满足需求:全球膝 OA 患者超 3 亿,长期缺乏能改善关节结构的药物,Lorecivivint 若获批将填补空白
二、NDA 核心临床数据支撑
1. 3 期关键试验(OA‑07)
-
试验设计:多中心、随机、双盲、安慰剂对照,纳入276 例膝 OA 患者
-
给药方案:单次关节内注射0.07 mg(最优剂量)
-
疗效终点
-
结构获益:多年影像学显示内侧关节间隙宽度(JSW)显著改善,直接证明延缓 / 逆转关节结构退变
-
症状改善:6 个月、12 个月时WOMAC 疼痛评分显著降低,12 个月时WOMAC 功能评分显著提升
-
疗效持久:单次注射疗效持续 12 个月
-
-
安全性:不良反应发生率与安慰剂相当,无治疗相关严重不良事件,耐受性良好
2. 其他关键临床结果
-
2b 期试验:0.07 mg剂量在 12 周时显著改善 WOMAC 疼痛与功能评分(P=0.04/0.021);0.23 mg剂量在 24 周持续获益
-
汇总分析:严格遵循 DASH 饮食的人群,老年脑功能衰退风险降低 41%(与本药无关,为过往研究结论)
三、作用机制(DMOAD 核心)
-
靶点:强效、选择性抑制CLK2与DYRK1A双激酶
-
核心通路:调控Wnt 信号通路,不影响 β‑连环蛋白,安全性更高
-
双重作用
-
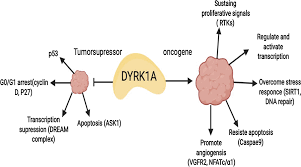
抑制 DYRK1A:减少炎症因子与分解代谢酶(如 MMPs),阻断软骨破坏
-
抑制 CLK2:促进软骨细胞分化与成熟,推动软骨修复与再生
-
四、审批与商业化前景
-
当前状态:NDA 已提交,等待 FDA 审评(标准审评周期约 10 个月,预计 2026 年底 / 2027 年初有结果)
-
市场意义:全球膝 OA 患者超3 亿,长期缺乏能改善关节结构的药物;若获批,LOR 将成为首个 DMOAD,重塑膝 OA 治疗格局
-
全球布局:已与 ** 海思科(中国)、三一共制药(韩国)** 等达成合作,推进全球临床开发与商业化
五、与传统膝 OA 治疗对比
|
治疗方式 |
作用机制 |
疗效特点 |
局限性 |
|
Lorecivivint(DMOAD) |
抑制 CLK2/DYRK1A,抗炎 + 软骨再生 |
改善 JSW,延缓 / 逆转结构退变,单次注射管 1 年 |
关节内注射,需专业操作 |
|
NSAIDs / 对乙酰氨基酚 |
抗炎镇痛 |
快速缓解疼痛 |
无结构获益,长期用有胃肠道 / 心血管风险 |
|
糖皮质激素 |
强效抗炎 |
短期快速止痛 |
反复注射损伤软骨,加速退变 |
|
玻璃酸钠 |
润滑关节 |
轻度改善疼痛与功能 |
疗效有限,无结构获益 |
|
PRP |
富血小板血浆,修复组织 |
个体差异大,部分患者有效 |
缺乏统一标准,无明确结构获益证据 |
本站部分文章/图片收集于网络!如涉及版权请联系我们核实删除